|
الذرة
ومكوناتها
العدد الكتلي أو عدد الكتلة(1)
بما أن البروتون
والنيوترون أثقل بكثير من الإلكترون
كما ذكرنا سابقا ، لذلك يمكن إهمال كتلة الإلكترون عند الحديث عن الكتلة
الذرية .
وضع
الكيميائيون مفهوما أسموه
العدد الكتلي
وهو
عدد صحيح مجرد (ليس له وحدة) .
يمثل العدد الكتلي مجموع
عدد البروتونات والنيوترونات الموجودة في نواة ذرة العنصرانظر إلى جدولك الدوري تجد في مربعات العناصر
التالية :
|
البروم |
الحديد |
الألمنيوم |
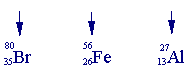 |
 تمرين (1) :
أكمل الفراغ في العبارتين التاليتين :
تمرين (1) :
أكمل الفراغ في العبارتين التاليتين :
 العدد الموضوع
اسفل رمز العنصر والى
يساره هو
عدده الذري
وهو عدد ــــ الموجودة في نواة ذرته .
العدد الموضوع
اسفل رمز العنصر والى
يساره هو
عدده الذري
وهو عدد ــــ الموجودة في نواة ذرته .
 العدد الموضوع
أعلى رمز العنصر والى
يساره وهو
العدد الكتلي
وهو مجموع عدد ــــ و ــــــ في نواة ذرته .
العدد الموضوع
أعلى رمز العنصر والى
يساره وهو
العدد الكتلي
وهو مجموع عدد ــــ و ــــــ في نواة ذرته .
 تمرين (2) :
تمرين (2) :
أكمل الجدول التالي مستعيناً
بالجدول الدوري :
|
عدده الكتلي |
عدده الذري |
رمزه |
اسم العنصر |
| |
|
|
الكبريت |
|
|
i53i |
|
|
|
i23i |
|
|
|
| |
|
|
القصدير |
| |
|
|
|
 تمرين (3) :
اكمل
الجدول التالي :
تمرين (3) :
اكمل
الجدول التالي :
|
عدد النيوترونات |
عدد البروتونات |
رمز العنصر |
عدد النيوترونات |
عدد البروتونات |
رمز
العنصر |
| |
|
3517Cl |
|
|
199F |
| |
|
5224Cr |
|
|
4018Ar |
| |
|
2412Mg |
|
|
20080Hg |
 تمرين (4) :
تمرين (4) :
الأشكال التالية تمثل أنوية
ذرات:
حدد العدد الذري والعدد الكتلي
وعدد الإلكترونات لكل ذرة منها في حالة التعادل.
اضغط هنا لمعرفة
الإجابة

اكتبوا لنا ملاحظاتكم
واستفساراتكم
|

